Über die Roile des Eisens in der Atmung des Seeigeleis. (B. 4) 15
c) Bei der Reaktion bildet sich keine Kohlensäure.
d) Wie die spontane Oxydation des Lecithins ist auch die
durch Eisen beschleunigte von einer Abnahme des Jodbindungs-
vermögens begleitet; und zwar wird ein Mehrfaches der-
jenigen Sauerstoffmenge aufgenommen, die zur Überfüh-
rung der verschwundenen Doppelbindungen
CH CHOH
II in genügte.
CH CHOH
] 0
e) Von den Beeinflussungen der Oxydationsgeschwindigkeit
ist wichtig, daß Säuren — Essigsäure, Buttersäure, Salzsäure,
Phosphorsäure, Schwefeisäure — sehr erheblich beschleuni-
gend wirken. (Deshalb wurde in der oben gegebenen Vorschrift
nicht Wasser, sondern ^üoo'Essigsäure als Milieu empfohlen.)
2. Linolensäure (CigHgoOg, Fettsäure mit 3 Doppelbindun-
gen; Molekulargewicht 278) ist von den Spaitungsprodukten des
Lecithins das einzige, dessen Oxydation durch Eisensaiz beschleu-
nigt wird; höchstwahrscheinlich setzt demnach die Lecithin-
oxydation an der Linolensäurekomponente ein.
a) Was die Mengenverhäitnisse anbetrifft, in cienen zweck-
mäßigerweise Säure, Eisen und Wasser zum Nachweis der Katalyse
gemischt werden, so giit dasselbe, was für das System Fe-Lecithin
gesagt wurde: wenig Substrat und viel Katalysator.
Wie das Lecithin, biidet auch die Linolensäure feine unci dauer-
hafte Emulsionen, wenn ihre methylalkoholische Lösung in Wasser
einnenossenwird. Eswurden
aiso 0,1 ccm Säure, in 5 ccm
Methylalkohoi gelöst, in ^
200 ccm MAsser gegossen. ^
In2ccmderEmulsionwaren ^
dann 0,9 mg Linolensäure. ^ ^ ^
Je 2 ccm wurden in ein At- ^
mungsgläschen pipettiert,
in eins außerdem 0,1 ccm
0,8%ige Lösung von MoHR- ^
schemSaiz(=0,lmgFe"). ^ ^
Bei 16^ wurden dann für den
f!
-
-
-
/
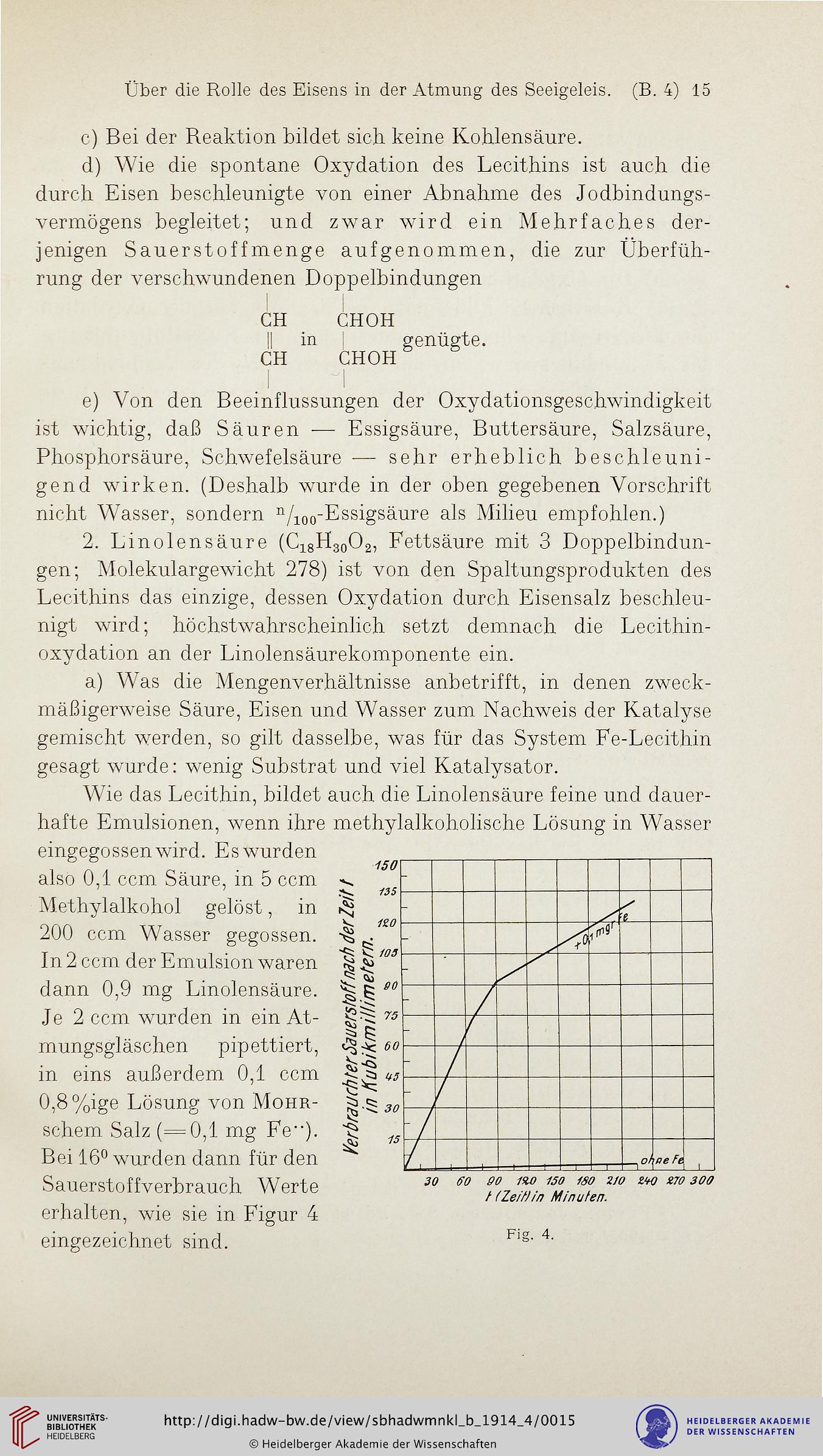
Sauerstoffverbrauch Werte
erhalten, wie sie in Figur 4
eingezeichnet sind.
J<7 W /X/7 /J/7 /y<7 ^7/7
/ /ZFW//7 /tf/'/7f/f/7.
Fig. 4.
c) Bei der Reaktion bildet sich keine Kohlensäure.
d) Wie die spontane Oxydation des Lecithins ist auch die
durch Eisen beschleunigte von einer Abnahme des Jodbindungs-
vermögens begleitet; und zwar wird ein Mehrfaches der-
jenigen Sauerstoffmenge aufgenommen, die zur Überfüh-
rung der verschwundenen Doppelbindungen
CH CHOH
II in genügte.
CH CHOH
] 0
e) Von den Beeinflussungen der Oxydationsgeschwindigkeit
ist wichtig, daß Säuren — Essigsäure, Buttersäure, Salzsäure,
Phosphorsäure, Schwefeisäure — sehr erheblich beschleuni-
gend wirken. (Deshalb wurde in der oben gegebenen Vorschrift
nicht Wasser, sondern ^üoo'Essigsäure als Milieu empfohlen.)
2. Linolensäure (CigHgoOg, Fettsäure mit 3 Doppelbindun-
gen; Molekulargewicht 278) ist von den Spaitungsprodukten des
Lecithins das einzige, dessen Oxydation durch Eisensaiz beschleu-
nigt wird; höchstwahrscheinlich setzt demnach die Lecithin-
oxydation an der Linolensäurekomponente ein.
a) Was die Mengenverhäitnisse anbetrifft, in cienen zweck-
mäßigerweise Säure, Eisen und Wasser zum Nachweis der Katalyse
gemischt werden, so giit dasselbe, was für das System Fe-Lecithin
gesagt wurde: wenig Substrat und viel Katalysator.
Wie das Lecithin, biidet auch die Linolensäure feine unci dauer-
hafte Emulsionen, wenn ihre methylalkoholische Lösung in Wasser
einnenossenwird. Eswurden
aiso 0,1 ccm Säure, in 5 ccm
Methylalkohoi gelöst, in ^
200 ccm MAsser gegossen. ^
In2ccmderEmulsionwaren ^
dann 0,9 mg Linolensäure. ^ ^ ^
Je 2 ccm wurden in ein At- ^
mungsgläschen pipettiert,
in eins außerdem 0,1 ccm
0,8%ige Lösung von MoHR- ^
schemSaiz(=0,lmgFe"). ^ ^
Bei 16^ wurden dann für den
f!
-
-
-
/
Sauerstoffverbrauch Werte
erhalten, wie sie in Figur 4
eingezeichnet sind.
J<7 W /X/7 /J/7 /y<7 ^7/7
/ /ZFW//7 /tf/'/7f/f/7.
Fig. 4.